6. ALTERACIONES CARDIOVASCULARES EN EL SÍNDROME DE APNEA DEL SUEÑO
SAS y presión arterial sistémica
En condiciones normales, durante el sueño se produce una disminución del trabajo al que se encuentra sometido el sistema cardiovascular. Esta reducción en la carga de trabajo se manifiesta por cambios en la presión arterial, frecuencia cardíaca y gasto cardíaco (Fletcher 1995). Con el desarrollo de tecnología automatizada y ambulatoria para la monitorización de la presión arterial, actualmente es posible el estudiar el perfil durante las 24 horas de esta variable fisiológica. Esta tecnología nos ha permitido observar que la presión arterial durante el día presenta valores medios superiores a los de la noche. La tensión arterial disminuye aproximadamente entre un 5-10% en las fases I y II, de un 10 a un 15% durante el sueño profundo. Durante la fase REM la presión arterial y la frecuencia cardiaca fluctúan. La actividad simpática disminuye progresivamente desde la fase de vigilia a la fase REM. El descenso en la tensión arterial durante el sueño se ha atribuido a una disminución en el gasto cardíaco, si bien una disminución de la resistencia vascular periférica podría también desempeñar un papel importante. Estas variaciones díanoche de la presión arterial pueden estar causadas por un ritmo circadiano interno y/o ser efecto directo del sueño. Existen diversos mecanismos implicados en la modulación de esa variabilidad de la presión arterial, como catecolaminas plasmáticas, sistema renina angiotensina y ADH, sistema nervioso simpático, movimientos ventilatorios así como los baroreceptores arteriales. Con respecto a este último mecanismo se ha observado, en algunos estudios, una relación inversa entre la sensibilidad del sistema baroreceptor y la variabilidad de la PA durante las 24 horas.
La presión arterial sistémica es una variable fisiológica, que va a tener una repercusión fundamental en la conservación de la integridad del sistema cardiovascular a largo plazo, por lo que toda alteración del sueño va a implicar una disminución del descanso que supone la noche para el sistema cardiovascular. Actualmente se conoce existen sujetos que no presentan disminución de la presión arterial sistémica durante la noche (sujetos nodipper), y que estos tienen mayor probabilidad de desarrollar problemas cardiovasculares (Suzuki et al. 1996). Entre ellos probablemente estaría un gran número de pacientes con SAS.
En los pacientes con SAS las apneas producen cuatro consecuencias fundamentales de importancia hemodinámica: 1) hipoxia progrexiva, dependiente de la duración de la apnea, volumen pulmonar y concentración basal de oxígeno; 2) progresiva hipercapnia, aún siendo esto considerablemente menos grave que la hipoxia, debido a la capacidad amortiguadora del organismo para el CO2; 3) presión negativa intratorácica generada por los esfuerzos del sistema ventilatorio en contra de la vía aérea cerrada y 4) microdespertar, lo cual conduce a restauración de la luz normal de la VAS y aparición de la ventilación (Weiss et al. 1996).
Al comienzo de la apnea, se produce una disminución de la PA, probablemente como resultado de la caída de la presión intratorácica. Al final de la apnea, la PA sube progresivamente con un pico al reiniciarse la ventilación y producirse el microdespertar. Después de este pico, la PA se mantiene elevada durante unos 10 15 segundos antes de volver a los valores normales.
Los principales mecanismos implicados en estas variaciones de la PA durante la apnea son la hipoxia, hipercapnia y despertares transitorios. En varios estudios se cita como fundamental a la hipoxia debido a las siguientes razones. Primero, el incremento de la PA antes del microdespertar se correlaciona con el grado de desaturación de oxígeno. Por otra parte el pico de PA, después del microdespertar, se correlaciona con la duración de la apnea. Segundo, la administración de oxígeno suplementario bloquea el incremento de la PA después de la apnea. En contraste con estos hallazgos, otros autores no han comprobado que el papel de la hipoxia sea el fundamental. En este sentido, la administración de oxígeno a flujos suficientes para mantener una saturación sanguínea mayor del 90% no previene las alteraciones hemodinámicas en relación con las apneas, por lo que actualmente se piensa que deben de existir otros factores asociados como son los II microdespertares II , los cambios en la presión intratorácica, y los fenómenos asociados a la reinflación del pulmón.
También existen datos publicados que implican al sistema nervioso simpático en las elevaciones de la presión arterial durante los episodios obstructivos. Hace 20 años, algunos autores observaron que los pacientes con síndrome de ShyDrager y enfermedad de Parkinson, los cuáles presentan alteraciones del sistema nervioso autónomo no elevaban su presión arterial sistémica en respuesta a las apneas obstructivas. Posteriormente, hace 10 años, la realización de registros de actividad simpática en pacientes con SAS permitió observar que las apneas obstructivas estaban asociadas con un progresivo incremento en la actividad del sistema nervioso simpático, seguido por una reducción brusca después de terminar la apnea. Usando técnicas similares, se ha comprobado que las apneas voluntarias inducen hipoxemia e incrementan la actividad simpática en sujetos normales. Además se ha observado niveles elevados de noradrenalina en plasma durante el sueño en pacientes con SAS e incrementos de estos niveles durante las apneas, correlacionándose con el grado de desaturación de oxígeno y disminuyendo tras el tratamiento del SAS con CPAP.
Por otra parte, la no disminución de la presión arterial durante la noche, así como las modificaciones cíclicas de la misma en relación con las apneas conduce a una sobrecarga ventricular izquierda que puede tener consecuencias clínicas. Algunos autores han documentado cómo los pacientes hipertensos con menos del 10% de reducción en la presión sanguínea nocturna tienen un índice de masa ventricular izquierda mayor que en los pacientes en los que la presión sanguínea desciende más del 10% en la noche. Es importante reconocer también que la presión transmural está incrementada no sólo por las elevaciones de la presión sistémica, sino también por la disminución de la presión intratorácica que acompaña a los esfuerzos respiratorios contra una VAS obstruida. Este último hecho ya fue sospechado hace 25 años por Lugaresi, quién demostró por cinefluoroscopia una «dilatación cardiaca aguda» durante las apneas obstructivas. Además de que la obstrucción de la VAS produce una presión intratorácica muy negativa que dificulta la contracción adecuada de ambos ventrículos (presiones transmurales elevadas), el aumento de la descarga del sistema nervioso simpático ocasiona un aumento importante de la postcarga de los ventrículos y del consumo de oxigeno por el miocardio, en un momento en que todo el organismo, y por tanto también el miocardio, se halla en una situación de hipoxia causada por la propia apnea.
Además el aumento de la presión negativa intratorácia incrementa el retorno venoso al lado derecho del corazón, con el resultado de distensión de la aurícula derecha. Este fenómeno puede incrementar la secreción de factor natriurético atrial que se ha puesto en relación con la nicturia presente en estos pacientes y que desaparece al comenzar el tratamiento con CPAP.
En consecuencia, puede afirmarse que el SAS da lugar a una sobrecarga crónica del sistema cardiovascular responsable, no solo de agravaciones de cardiopatías preexistentes, sino probablemente también de algunos casos de miocardiopatia que eran etiquetadas como esenciales. En definitiva los cambios agudos durante la apnearecuperación de la ventilación reflejan la respuesta integrada a estímulos como la hipoxia, hipercapnia, cambios en la presión intratorácica, en el volumen pulmonar y despertares transitorios (Figura 3).
El proceso por el cual los pacientes con SAS mantienen durante el día presiones arteriales sistémicas elevadas (Brooks et al. 1997) es un proceso que también está bajo discusión. Es posible que los episodios repetidos de desaturación nocturna y de elevación de la presión arterial conduzcan a la producción de lesión estructural vascular permanente en los pacientes con SAS. También se ha postulado la presencia de un defecto en la sensibilidad de los quimioreceptores periféricos, sistema reninaangiotensinaaldostena o al factor natriurético atrial. Incluso se ha descrito una disminución de algunos factores endoteliales vasodilatadores, como el oxido nítrico.
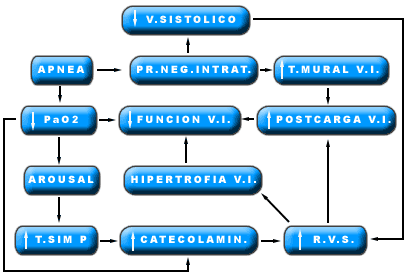
Figura 3
Cambios hemodinámicos durante el ciclo apnea/recuperación
SAS y frecuencia cardíaca
La frecuencia cardíaca disminuye un 10-25% durante el sueño en relación a la vigilia y este decremento es mediada por el sistema vagal. Esta disminución de la frecuencia cardíaca condiciona una reducción del gasto cardíaco. La frecuencia cardiaca aumenta durante la apnea y se incrementa fuertemente al terminar ésta, en relación con el despertar transitorio y el comienzo de la ventilación.
Es conocido también que durante el sueño se producen alteraciones del ritmo cardíaco, siendo la bradicardia la arritmia más común. Existe una variación cíclica del ritmo cardíaco en los pacientes son SAS en relación con la duración de la apnea y la severidad de la desaturación de la hemoglobina. Aunque las variaciones cíclicas en la frecuencia cardíaca deben poner al clínico ante la sospecha de SAS, este hallazgo no es diagnostico, y su ausencia no excluye el mismo.
También han sido descritas pausas sinusales, extrasístoles ventriculares y bloqueo auriculoventricular de segundo grado en los pacientes con SAS. Con desaturaciones menores del 60% se producen frecuentemente incrementos de los complejos ventriculares prematuros o episodios de taquicardia ventricular que no se presentan durante la vigilia.
SAS y enfermedades cardiovasculares. Estudios epidemiológicos
La relación entre el SAS y las enfermedades cardiovasculares se ha discutido enormemente en los estudios epidemiológicos (Wright et al. 1997). En torno al 40% de los pacientes con SAS tienen HTA sistémica mientras que la prevalencia del SAS es alrededor del 30% de los pacientes hipertensos, y oscila entre el 0 y 13% en pacientes normotensos. Varios autores han descrito la reducción de la presión arterial tras el tratamiento del SAS.
También se ha observado asociación con la enfermedad coronaria. En 1982, De Olazábal demuestra que los enfermos con enfermedad coronaria presentan frecuentemente desaturaciones de oxígeno nocturnas y apneas. Posteriormente estudios realizados en Australia por Hung (1990) encuentra una asociación significativa entre SAS e infarto de miocardio, independientemente de la edad, BMI, hipertensión arterial, hábito de fumar y nivel de colesterol sanguíneo, existiendo un incremento en el riesgo de infarto de miocardio a medida que se incrementan los niveles de índice apneahipopnea.
En un estudio prospectivo de 4 años, incluso el ronquido se ha visto que puede estar relacionado con el desarrollo de cardiopatía isquémica (Zamarrón et al. 1999). También se ha comprobado, en sujetos con SAS que ingresan en una Unidad de Cuidados Intensivos por infarto de miocardio, que el número de arritmias cardíacas es mayor que en los sujetos que no presentan SAS.

